연세대 치과대학(학장 김의성) 최성환 교정과학교실 교수, 권재성 치과생체재료공학교실 교수, 연세대 공과대학(학장 명재민) 홍진기 화공생명공학과 교수 연구팀이 12월 10일 충치 치료 시 치아의 재생 능력을 높일 수 있는 재료를 개발했다.
이번 <다가 양극성 네트워크 개질제를 통해 생체 활성이 상향 조절된 바이오필름 저항성 폴리알케노에이트 시멘트의 개발(Multivalent network modifier upregulates bioactivity of multispecies biofilm-resistant polyalkenoate cement)> 논문은 최근 생체 재료 분야 국제 학술지 ‘Bioactive Materials(IF 14.593)’에 게재됐다.
치과에서 충치로 손상된 치아의 치료를 위해서는 ‘폴리알케노에이트 시멘트(PAC)’라 불리는 재료를 활용한다. 충치 부위를 제거하고 PAC을 채우면 체내에서 칼슘, 불소 등과 같은 다양한 이온들이 방출돼 치아 경조직의 재생이 촉진되는 특성을 활용한 것이다.
PAC의 대표적인 예로 ‘글래스 아이오노머 시멘트’가 있다. 글래스 아이오노머 시멘트의 경우 충치 부위를 제거한 후 채워 넣었을 때 생체 내에서 불소 이온 방출을 통한 충치 예방 효과가 높은 장점이 있었다.
연구팀은 기존의 PAC보다 더 다양하고 이로운 이온들(특히 칼슘, 인, 스트론튬)의 방출량을 높인 재료를 개발하고자 했다. 이에 mZM(multivalent zwitterionic network modifier, 다가 양극성 네트워크 개질제)을 적용한 zPAC(zwitterionic PAC)을 개발하는 데 성공했다.
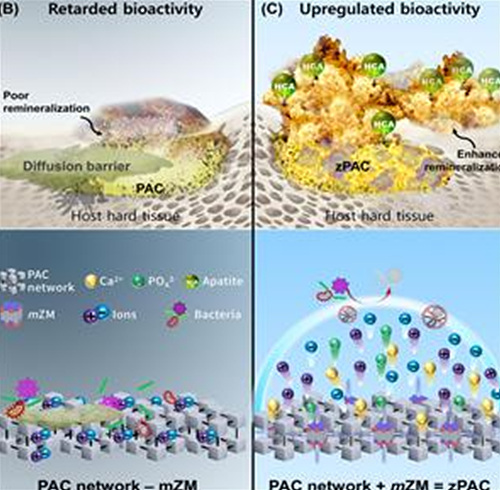
PAC의 주된 구성물은 이산화규소(SiO2)로 망상 네트워크를 구성한 실리카 유리다. 이산화규소로 이뤄진 망상 네트워크 안에서 비가교 산소(non-briging oxygen)/가교 산소(briging oxygen) 비율이 증가하면 충분한 이온이 방출될 수 있는 환경이 조성된다.
현재까지는 이 네트워크 내 비가교 산소/가교 산소의 비율을 조절하기 위해 단순히 양전하(+)만을 가진 금속 이온만을 활용해 왔으나 이는 비가교 산소/가교 산소 비율을 증가시키는 효율이 낮다는 한계가 있었다. 또한 PAC 표면이 세균성 바이오필름으로 오염되는 경우 이온 방출 자체가 차단되는 현상도 관찰됐다.
연구팀은 이 같은 문제점에 착안해 PAC 내 이온이 충분히 방출될 수 있는 환경을 조성했다. 새롭게 개발한 zPAC은 양전하(+)와 음전하(-) 모두를 가진 양극성 이온(쯔비터 이온)을 사용해 망상 네트워크 안 산소와의 반응률을 높여 비가교 산소/가교 산소의 비율을 높였다. 또한 양극성 이온이 지닌 표면 수막 형성능을 이용해 PAC 표면 바이오필름의 생성도 억제했다.
실제로 생체를 모사한 환경에서, 개발된 zPAC은 기존의 PAC에서는 거의 방출되지 않았던 칼슘과 인을 포함한 다양한 이온의 방출을 증가시켰으며 치아 경조직의 대부분을 이루는 ‘하이드록시아파타이트’ 무기물의 PAC 표면 침착을 약 74% 증가시키는 것으로 나타났다. 이와 함께 기존의 PAC과 달리 zPAC에서 방출된 이온들은 인간 치수 줄기세포의 분화를 촉진해 치수 줄기세포에 의한 경조직 생성 또한 증가시키는 것으로 확인됐다.
성견을 이용한 중대형 동물 모델에서도 zPAC을 충전한 치아에서 경조직 침착을 확인할 수 있었고, zPAC 표면의 세균성 바이오필름의 부착 또한 약 68% 감소하는 것으로 나타났다. 동시에 zPAC 표면에 부착된 바이오필름을 구성하는 미생물 종의 분포 또한 정상화되는 것으로 분석됐다.
최성환 교정과학교실 교수는 “zPAC은 치의학을 넘어 재생의학 분야에도 널리 적용될 수 있는 유망한 솔루션이 될 수 있을 것”이라며 “이를 통해 손상된 치아 또는 골조직의 재광화가 보다 쉽게 이뤄질 수 있다는 점에서 의미가 크다”고 말했다.
한편 이번 연구는 한국연구재단과 범부처전주기의료기기개발사업 및 연세대 치과대학-공과대학 연구증진 사업의 지원으로 수행됐다.