임플란트 표면에 대한 이해

최근 임플란트를 이용한 치료가 치과치료의 광범위한 부분을 차지하면서 수종의 임플란트가 개발되어 시판되고 있으며 여러 임플란트 회사들은 각자의 표면처리 방식의 우수성을 증명하기 위하여 많은 비교 연구들을 시행하고 있다. 이러한 연구들은 표면처리 개발의 차원에서는 긍정적인 영향을 준 반면, 실질적으로 임플란트를 사용하는 임상의에게는 혼란을 주기도 한다. 따라서 임플란트 표면에 대한 골유착 반응을 알고 최근 시판되고 있는 임플란트 표면에 대한 이해가 우선되어야 할 것이다. 이에 임플란트 골유착에 대한 기본적인 내용과 더불어 현재 조선대학교 치과병원 임플란트 센타에서 주로 사용하는 임플란트 시스템을 기준으로 표면처리에 대해 정리하고자 한다.
1. 임플란트 골유착의 과정
임플란트의 전체적인 안정성은 초기고정과 이차고정 과정의 연속으로서 얻어질 수 있다. 임플란트 식립시 기존골과 식립된 임플란트 사이의 fit에 의해 형성되는 고정을 초기고정 (또는 일차고정, primary stability )이라 한다. 이는 골질의 상태나 수술시 드릴링의 정확성, 임플란트 고정체의 모양등에 의해 영향을 받으며 식립 후 약 4주간에 걸쳐 임플란트를 고정한다. 반면 임플란트 식립후 시간이 지남에 따라 새로운 골이 임플란트와 기존 골사이 계면에 형성됨으로서 생성되는 고정을 이차고정(secondary stability) 이라 한다. 일반적으로 임플란트의 골 유착이라 함은 이러한 이차고정의 유무와 정도의 표현이라 할수 있다. 따라서 임플란트의 표면처리는 이러한 이차고정에 영향을 미치는 주요한 요인이라 할 수 있다.

2. 골유착의 단계
임플란트 식립 후 나타나는 골유착의 단계는 1st stage, 2nd stage, 3rd stage로 나눌 수 있으며 이는 골친화기, 골전도기, 골적응기로 각각 분류되기도 한다. 1st stage는 임플란트 식립후 woven bone이 형성되기까지의 약 1달 정도의 기간이라 할 수 있다. 임플란트 식립후 임플란트와 골사이에 일어나는 과정은 창상으로 인한 골 치유반응과 유사하다. 즉, 임플란트와 골 사이에 혈액이 차고, 혈병(blood clot)이 형성되며 혈병의 분해와 함께 fibrin network이 형성된다. 식립 1주내에 임플란트 표면내로 골아 세포들이 이주하여 골화가 시작되고 임플란트 식립 시 압축된 골의 초기흡수가 일어나고 BMP가 유리되며 이에 반응하여 세포이주가 일어난다. 임플란트 표면에 접근한 골 세포들은 유골(osteoid)을 형성하고 이는 미성숙 결합 조직기질로서 여기에 woven bone이 침착되게 된다. 2nd stage는 woven bone 이 더 강한 성숙골인 lamellar bone으로 치환되는 과정으로 2-3개월에 걸쳐 진행되며 임플란트 표면에 더 많은 양의 골이 더해지는 단계이다. 3rd stage는 식립후 3-4개월 이후부터 더 이상의 골 접촉은 증가하거나 감소하지 않고 부하에 반응하여 bone remodeling 이 전 생애에 걸쳐 일어나는 단계라 할 수 있다. 이러한 골유착의 과정들은 임플란트 표면에 골의 접촉이 일어나야하고 이를 위해서는 임플란트 표면에 세포의 부착이 우선되어야 한다. 골유착에 대한 임플란트 표면처리의 효과는 1) fibrin attachment를 증가시키고 2) 혈병의 형성을 안정화하며 3) 세포의 이주와 분화를 촉진시킴으로서 임플란트 주변의 초기 bone healing에 영향을 준다.

3. 임플란트 표면처리
초기 임플란트 표면형태인 machined surface는 장기간의 데이터를 가지고 그 성공률에서도 훌륭했지만 임플란트의 임상에의 응용이 골질이 나쁜 경우, 골 이식이 필요한 경우, 그리고 즉시하중을 요구하는 증례 등 점차적으로 더 복잡하고 어려운 증례에서의 사용으로 그 응용의 폭이 넓어짐에 따라 더 빠른 골 유착을 유도하기 위해 rough Surface가 개발되었다. rough Surface는 티타늄 분말이나 수산화 인회석을 임플란트 표면에 부착시키는 Additive method와 blasting, etching등을 이용하여 표면자체에 거칠기를 형성하는 Subtractive method로 나눌수 있다. 과거 plasma spraying을 이용하여 티타늄 분말이나 HA 분말을 부착시키던 방법은 표면적을 증가시키고 초기 임플란트 안정성을 증가시키며 더 강한 골-임플란트 계면을 형성했던 장점이 있었던 반면, 코팅방법에 따라 차이가 많이 나고 고온 분사에 따라 기존기질의 변화가 야기될 수 있으며 코팅의 분리 및 균일하지 않은 코팅 형성등이 문제가 되었고 임플란트 계면으로부터 탈락된 코팅 알갱이들이 감염원으로 작용하는 문제점들도 지적되었다. 이러한 코팅법의 문제를 개선하기 위해 코팅기법을 달리하거나 표면을 변화시킴으로서 거칠기를 형성하는 다양한 방법이 소개되었다. 산화티타늄이나 CaP를 이용하여 표면을 blasting하거나 염산이나 황산을 이용하여 etching하는 방법, 또는 이를 병행하는 방법등 임플란트 회사별로 각각의 특수 표면처리 기법을 소개하고 있다.
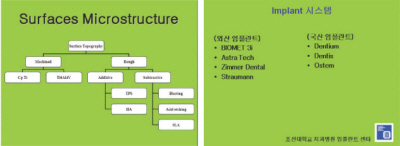
다음은 조선대학교 치과병원 임플란트 센타에서 주로 사용하는 임플란트 시스템으로서 외산과 국산 임플란트로 구분하여 각각의 표면처리에 대해 정리해 보았다.
4 각종 임플란트 시스템의 표면처리
1) BIOMET 3i
(1) OsseoTite
3i의 OsseoTite는 순수티타늄이나 티타늄합금에 염산(HCl)과 황산(H2SO4)을 사용하여 dual acid etching함으로서 표면의 미세 거칠기를 형성하였다. 1998년 Davis등은 OsseoTite surface가 더 강한 혈병의 부착을 유도하고 osteogenic response를 증가시킨다고 보고한바 있다.

2) NanoTite
최근 3i는 NanoTite 표면을 소개하였다. 이는 기존의 OsseoTite 표면에 20-100 nm의 Calcium Phosphate(CaP) 결정이 분산되어 침착되어 있으며 이는 일반적인 HA 코팅보다 전단력이 강하다.
2) Astra Tech
(1)TiOblast
기존의 Astra 임플란트는 TiOblast이다. 이는 TiO2로 임플란트 표면을 Grit blasting한 표면이다.
(2) OsseoSpeed
TiOblast 임플란트 표면에 불소처리를 하여 잇몸 뼈와 임플란트가 유착되는 기간을 최소화하여 치료기간을 단축시키기 위해 개발된 임플란트가 OsseoSpeed 이다. 즉 TiO2로 blast처리된 티타늄의 산화층에 소량의 불소이온이 병합됨으로서 표면 거칠기가 약간 더 증가되고 nanoscale의 표면구조가 생긴다는 것이다.

3) Zimmer Dental
(1) MTX (Microtextured Titanium Surface)
HA 분말로 임플란트 표면을 grit blasting하고 non etching acid로 세척하는 방법이다. 이는 acid etching이 아니므로 절삭면등을 그대로 보존할 수 있어 효율적인 절삭력을 갖는 장점이 있다.
2) MP-1 (HA coating surface)
HA surface로서 이는 일반적인 plasma spray처리 후 일정기압을 유지한 상태에서 열수 처리하여 순수 crystallin HA를 97% 까지 증가시킨 방법이다. 일반적으로 HA 코팅방법이 코팅기술이 부족하고 무정형 칼슘인산의 비율이 높아 발생되는 단점을 보완하고 HA의 우수한 성질을 이용하기위해 개발된 방법이다.
이러한 두가지 표면방법은 Zimmer implant 시스템이 적용되고 있는데 Screvent의 경우는 두가지 표면이 공급되어 선택적으로 사용할 수 있고, Tapered Screw-Vent는 연조직 반응이 중요한 상부는 MTX, 골유착이 중요한 중간부위는 HA, 절삭력이 중요한 근단부는 MTX로 구성되는 dual transitional type이 보급되고 있다.

4) Straumann Implant
Straumann 임플란트는 1974년 rough surface의 개발에 앞장서 TPS 방법의 임플란트를 소개하였고 1991년 SLA, 2005년 SLActive표면에 이르기까지 표면처리기법의 선두를 달리는 임플란트중의 하나이다.
(1)SLA (Sand blasted, Large grit, Acid etched)
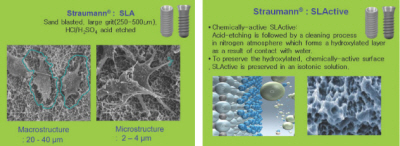
이는 Sand blasting한 후 250-500um의 large grit으로 표면 거칠기를 형성하고 염산과 황산으로 etching한 표면이다. 이는 20-40um의 거대 다공성과 더불어 2-4um의 소다공성 구조를 갖는 표면구조 양상을 보인다.
(2)SLActive
대부분의 임플란트가 첫 8주내에 실패가 야기되므로 초기 임플란트 치유과정에서 더 우수한 표면을 만들고자 하는 시도에서 비롯되어 개발되었다. 즉, 임플란트 골유착의 일차고정과 이차고정사이의 기간에 있어서의 차이를 줄이고자 빠른 2차 고정을 유도함으로서 임플란트 실패를 줄인다는 이론이다.
SLA 임플란트 표면처리의 마지막 단계인 etching후 질소상태에서 세척을 시행하고 이는 물과 접촉의 결과로 hydroxyl layer를 형성한다. 이는 positive charge되어 high surface energy를 갖게 되고 임플란트와 주변 환경과의 이상적인 접촉을 증가시킨다. activated된 표면은 보존되어 생리식염수가 들어있는 용기내에 보관되어 공급된다. 이때 음이온인 염소이온이 hydroxyl 이온과 결합하여 activate된 표면을 공기로부터 보호함으로써 hydrocarbon과의 결합을 방지하는 효과를 갖는다.
5) Dentis
Dentis 임플란트는 RBM 표면처리를 이용한 임플란트로서 독자적인 세척 시스템을 적용하여 blasting한후 잔여물이 남지 않게 완전히 제거함으로서 깨끗한 표면을 표방하는 CLEANANT 표면과 최근 상온 초박막 코팅법으로 HA를 코팅한 HAPTITE 표면이 소개되고 있다.

6) Osstem
HA 분말로 blasting한 RBM 표면처리 방법을 사용한다.

Blasting과 etching을 이용한 SLA 표면기법을 사용한다.

최근에도 많은 임플란트 회사에서 독자적인 표면처리 방법을 연구 개발하고 있다. 이는 임플란트 표면의 우수성이 곧 임플란트 성공률및 적용범위의 다양성에 직접적으로 영향을 줄수 있기 때문이라 생각된다. 이러한 표면처리 기법의 발전에 앞서 우선되어야 할 것은 골유착의 기전을 이해하고 스스로 사용하고 있는 시스템의 임플란트 표면이 어떤 처리방법을 사용하고 있는지 정리해 보는 시간이 필요하리가 사료된다.
** 본 글이 사용된 일부 슬라이드와 표면처리 사진은 각 임플란트 시스템의 교육용 자료에서 발췌하였습니다.
진보된 임플란트 표면 특성

임플란트의 등장은 치의학의 새로운 전기가 될 정도로 큰 변화를 가져 왔다. 혈관재생 과정을 연구하기 위해 티타늄을 토끼 경골에 이식했던 Br?nemark이 우수한 생체 안정성을 가진 티타늄이 아니라 다른 금속을 사용했더라면 골유착을 발견할 수 없었을지도 모른다. 혹은 그 당시 스웨덴에서 가장 흔했던 티타늄 로드의 직경이 5 mm가 아니었더라면 현재와 같이 3.75 mm가 regular diameter로 광범위하게 사용되지 않았을 수도 있었을 것이다. 초기 이러한 우연의 반복에 의해 개시되었던 임플란트는 조심스러운 임상적 성공을 거쳐 눈부시게 진화를 거듭하고 있다. 이제는 누구나 임플란트의 성공을 의심치 않지만 모든 증례에서 성공하는 것은 아니며 아직도 골질이 나쁜 경우 90% 미만의 성공률을 기록한다고 보고되고 있어 임상적 성공률을 조금이라도 향상시키기 위한 연구가 지속적으로 진행되고 있다.
임플란트의 성공을 위한 조건으로 Albrektsson (1982)이 제시한 6가지 조건 중 초기의 임플란트 시술에 비해 임플란트 디자인, 하중의 시기, 수술기법의 발전, 표면의 성질 등은 초기의 개념과는 현저한 차이를 보인다. 다른 조건들이 어느 정도 확립된 이론의 진전을 이룬 반면 임플란트 표면성질이라는 부분에서는 아직도 달성가능한 부분의 일부만 점령되고 있다고 할 수 있다.
임플란트 표면은 티타늄이 공기 중에 노출될 때 자연적으로 생기는 티타늄 산화막 (TiO2)의 생체 안정성에 의해 생체 내에서 이물 반응을 일으키지 않고 안정적으로 기능할 수 있다. 하지만 기계절삭형인 임플란트 표면만으로는 더 높은 성공률과 더 강한 골유착을 원하는 임상가들을 만족시킬 수가 없었다. 1990년대에 진행된 다양한 연구에 의해 적당한 거칠기를 임플란트 표면에 부여함으로써 우수한 골반응을 유도할 수 있다는 이론이 정립됨에 따라 1.0 - 1.5 μm의 적절히 거친 (moderately roughened) 표면을 만들 수 있는 표면개질법이 시도되었다. 티타늄 플라즈마 코팅이나 HA 코팅이 생체 내에서 분해되고 실패하는 한계가 드러나면서 티타늄 표면에 알루미나 분말을 분사하거나 티타늄 옥사이드 분말 또는 칼슘 포스페이트 분말을 분사하는 방법, 강산을 이용한 이중 산부식법을 이용하는 방법, 알루미나 분말을 분사한 후 산처리를 하는 복합법 등이 시도되었고 2000년대에는 더 이상 기계절삭형 임플란트를 임상적으로 추천하지 않고 있다. 표면조도가 적절히 개질된 임플란트의 우수한 골반응으로 인해 임상가들은 더 짧은 임플란트를 부족한 골량을 가진 환자에게 시도할 수 있게 되었으며 치유 기간도 더욱 단축시킬 수 있게 되었다.
하지만 임플란트의 표면 특성은 위에서 언급한 표면조도 외에도 규정할 수 있는 특성이 있기 때문에 표면 특성을 표면조도에 국한하지 말고 5가지 독립된 특성으로 나누어 평가해야 한다.
1) 표면조도 (표면의 지형학적 특성)
2) 티타늄 산화막의 두께
3) 결정 구조
4) 표면의 다공성 (기공의 크기 및 연결도)
5) 표면의 화학적 조성
표면조도가 1990년대에 활발하게 진행되었다면 현재는 다른 요소들이 골유착에 미치는 영향에 대한 연구가 많다. 먼저 티타늄 산화막은 티타늄이 공기 중에 노출될 때 자연스럽게 3-17 nm 정도의 두께로 형성되어 티타늄의 생체 불활성(bioinert)한 성질의 key factor가 된다. 그런데 양극산화(anodic oxidation)을 이용하면 티타늄 산화막의 두께는 자연 산화막의 두께를 10,000nm까지 증가시킬 수 있는데 이렇게 티타늄 산화막의 생활성을 이용한 임플란트로는 TiUnite (Nobelbiocare)을 들 수 있다. 최근 M (신흥) 임플란트는 산화막의 두께를 3,400-4,000nm의 일정한 두께로 제한하여 산화막의 최적 두께에 관한 최적점을 제시하였다.
티타늄의 결정구조 또한 양극산화 방식을 이용하면 기계절삭형이나 대부분의 임플란트에서 나타나는 무정형 티타늄구조에 비해 양극산화 임플란트에서는 Anatase와 함께 Rutile 구조까지 높은 빈도로 나타나고 있으며 이러한 Anatase와 Rutile 혼합형 결정 구조가 골반응에 최적의 조건이라는 것이 증명된 바 있다. 표면의 조도와 함께 다공성 즉 기공(pore)구조도 골조직이 자라 들어가 강력한 골유착을 이루는데 기여할 수 있다 (Figure 1).
하지만 최근에 가장 큰 이슈가 되고 있는 것은 표면의 화학적 조성을 변화시키는 것에 관한 부분이다. 그 예로는 열처리를 동반한 NaOH 처리법과 불소처리법, 양극산화법 및 이온주입법 등을 들 수 있다. 열처리를 동반한 NaOH 처리법을 이용하여 티타늄 표면에 인회석 층을 형성시킬 수 있다는 연구가 많지만 NaOH 처리 후의 표면의 불안정성 때문에 아직 임상용으로는 나오지 않고 있다. 불소(fluoride)처리법은 Ellingsen 등이 개발한 방법으로 Osseospeed (Astra tech)라는 임상 임플란트로 시판되고 있다. 이러한 불소 처리 임플란트는 불소함입에 의해 알칼리성 인산분해 효소의 분비를 촉진하고 수산화인회석 결정 형성을 촉진하며 HA보다 더욱 안정적인 fluoride-apatite를 형성하기 때문에 우수한 골반응을 나타내는 생화학적 표면처리법이라고 발표되었으나 그 효과가 실제 불소의 효과인지 표면의 125,000배 정도의 강확대 SEM 사진에서 확인되는 나노 단위의 조도변화에 의한 것인지는 아직 분별이 어렵다. 또 다른 화학적 성분 개질의 방법은 앞서 언급했던 양극산화법으로 마그네슘(Mg), 칼슘(Ca), 인(P) 등의 활성이온을 표면에 함입시킬 수 있기 때문에 양이온의 반응에 의해 초기 단백질의 응집 및 부착과 ligand 매개 세포반응을 촉진시킬 수 있다고 알려져 있다. Ca 함입 임플란트는 Ospol에서 출시되며 P 함입 임플란트는 TiUnite (Nobelbiocare), Mg 함입 임플란트는 M (신흥) 임플란트 등으로 시판되고 있다. 마지막으로 표면의 화학적 성질을 개질할 수 있는 방법이 이온주입법인데 표면에 이온을 주입함으로써 표면의 조도나 형태를 변화시키지 않으면서 이온 주입에 의한 생화학적 특성만 변화시키는 방법이다. 이 표면개질법도 아직 임상 임플란트로 시판되지는 않으나 국내 회사에서 임상시험 연구가 진행 중이다. 초기 HA 임플란트가 피복의 안정성이 낮아 시술 후 표면으로부터 해리되어 장기간의 안정성이 나빠 외면 받았던 것에 비해 최근의 HA coating은 피복의 기술이 현저히 발전하면서 생활성 유착의 강력한 증거를 실험실 연구 등으로 제시하고 있으므로 좀 더 장기적으로 지켜보아야 할 것이다.
그 외의 특성으로 표면에너지를 들 수 있는데 친수성(hydrophilicity)을 강화시켜 표면에너지를 증가시킴으로써 초기 혈액과의 반응속도를 증가시킨 SLActive (Straumann) 임플란트도 있다.
최근 마이크로미터 단위의 표면조도가 아닌 나노미터 단위의 표면조도에 주목하고 있는 연구가 많은데 이러한 나노단위의 구조는 초기 치유반응을 촉진시키며 matrix vesicle에 매개한 수산화인회석 결정의 nucleation site가 된다고 발표되었다 (Fig. 2). Nanotite (3i)나 Osseospeed (Astra tech) 등이 그 예가 될 터인데 많은 연구자들이 연구기법의 발전에 따라 나노 구조에 대한 연구를 지속하고 있어 이 분야에 대한 비약적인 발전을 기대해 본다.
이상과 같이 임플란트의 표면특성에 대한 연구는 아직도 무한한 가능성을 지니고 있어 앞으로의 임플란트 발전을 견인하는 주요한 도구가 될 것이다. 하지만 대부분의 표면 연구가 in vitro 실험이나 in vivo 동물 실험에 의한 것이 많아 성공적인 결과를 임상적으로 입증하지 못했다는 것이 주된 약점이므로 장기간의 임상적인 데이터로 치과의사들에게 신뢰를 입증해야 할 숙제를 가지고 있다.
Fig. 1 양극산화 임플란트에 의한 다공성 구조.
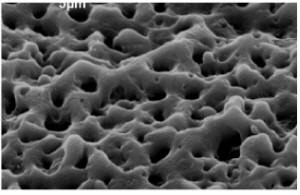
Fig. 2 좌측: sandblasting 임플란트
중간: Fluoride 처리 임플란트
우측 : nano HA 처리 임플란트
(Meirelles et al., Int J Oral Maxillofac Impl 2008에서 인용)

알파바이오 임플란트를 중심으로 본 즉시 부하의 성공 요인

Alpha -bio사는 1986년 이스라엘에서 설립된 임플란트 회사다. 2008년 Nobel biocare사와 합병된다. 합병이유는 Alpha-bio사의 즉시부하를 위해 특별히 디자인된 작은 직경의 ARRP(Arrow implant)를 통하여 임플란트 시장에서 가장 급성장하는 작은 직경의 임플란트부분에서 즉각 접근 할 수 있고 즉시 부하에 유리한 알파바이오사의 혁신적인 SFB를 기본 모델로 Nobel Active를 개발하기 위해서였다.
현재 Nobel Active는 출시 즉시 26만개가 판매 되었고 임플란트의 미래로 평가 받고 있다.
알파바이오는 Nobel Active와 같은 즉시부하에 유리한 SPI(Spiral Implant)와 좁은 골 뿐 아니라 모든 골 타입에 즉시 부하가 가능한 One piece 임플란트인 ARRP(Arrow implant), 그리고 DFI(Dualfit implant), ATID(Dual implant)등 알파 바이이오사의 모든 제품을 올해 상반기에 한국에 출시 했다.
알파바이오 임플란트를 한 마디로 말한 다면 간편함이다.
좋은 임플란트를 고안 하기위해서는 생물학과 기계역학에 관한 수많은 지식이 요구되며 이들을 잘 조화시켜야만 한다.
인체를 이해하고 골 생리를 이해하고 기계역학에 대한 해박한 지식을 바탕으로 개발된 빠르고 쉽고 편하고 간편한 임플란트, 자연치아를 가장 세련되게 대치하는 임플란트가 바로 알파바이오의 임플란트들이다.
알파바이오 임플란트 개발의 중심에는 Dr. Ophir Fromovich가 있었다. Dr. Ophir는 현재 노벨바이오케어의 Nobel Active의 연자로 활동 중이다. 필자가 Dr. Ophir를 처음 만난 것 은 2005년이었다. NobelActive의 전신인 SFB와 SPI, ARRP, DFI, ATID의 개념을 필자에게 오후 2시 부터 자정을 넘길 때까지 정말 지치지 않고 설명해 주었다. 그 당시 Dr. Ophir는 나에게 알파바이오 임플란트를 이용하여 즉시 로딩을 시도해보라고 강력하게 권하였다. 그 이후 필자는 그 의 병원을 수차례방문 하여 그가 시술하는 모습을 보며 알파임플란트에 대하여 놀라움과 확신을 갖게 되었고 그가 홍콩 태국 대만등 아시아지역에 강의를 올 때 그의 강의를 들었었다.
알파바이오가 즉시 부하에 유리한 이유는 강력한 초기 고정에 있다. 그리고 부하 분산이 매우 이상적인 구조를 가지고 있고 측방력에도 잘 견딜 수 있는 구조와 골을 보호하고 골 질을 개선시키는 구조를 가지고 있어서 기존의 임플란트에 비해서 즉시 로딩에 보다 유리하다.
즉시 부하가 필요한 경우 즉시 부하가 가능한 최소한의 골량이 요구 된다.
부하를 담당하는 곳은 임플란트가 아니라 골이기 때문이다. 임플란트가 아무리 두꺼워도 이를 견디는 골의 두께가 적절 하지 않으면 실패율이 높다.
즉 , 즉시 부하 성공의 KEY는 잔존골의 양과 질을 좀더 좋게 해야 하는 것이다.
아무리 골량이 적더라도 골질이 건전한 층판골이라면 즉시 부하는 가능하다. 골폭이 좁은 경우 지름이 더 작은 임플란트를 식립한다면 작은 골량이라 할 지라도 즉시 부하가 가능한 것이다. 골량이 풍부한 경우에도 작은 직경의 임플란트를 식립 할 경우 삭제된 골의 량이 적어 풍부한 골이 보존되어 하중을 담당하게 되므로 더욱 확실하게 즉시부하의 성공률이 높아진다고 할 수 있다
잔존 골량에 상관없이 가용한 최소 지름의 임플란트를 식립한다면 모든 경우에 가장 성공률이 높다고 예상할 수 있다.
즉 잔존 건전골이 많을 수록 즉시 부하의 성공률은 높아지는 원리다.
Spi와 ARRP는 모두 적은 직경의 drilling을 하고 굵은 임플란트를 즉시 식립 할 수 있기 때문에 즉시 식립 및 즉시 부하에 매우 유리한 임플란트이다.
ARRP는 테이퍼 하면서 Thread가 깊기 때문에 식립 이 쉽고 편하다.
전치와 소구치 뿐만 아니라 대구치에서도 발치 즉시 식립 및 즉시 부하가 가능한 임플란트이다.
과거에는 즉시 식립시 발치와에 맞는 임플란트를 식립하는 경향이 있었으나 발치후 골 흡수 양상을 고려할 때 많은 문제를 발생 시키기 때문에 최근에는 발치후에 즉시 식립 할 때 발치와 보다 적은 직경의 임플란트를 구개측 혹은 설측에 식립 하는 경향이 우세하다.
SPI와 ARRP는 높은 초기 고정력과 편한 식립이 특징이다. Apex 그리고 middle과 crest모든 부위에서 골 콘덴싱 기능이 있어 모든 부위에서 우수한 초기고정이 나오기에 complicate한 case에서도 즉시부하가 가능한 고정이 나온다.
그러나 초기 고정이 강하게 나오기 때문에 주의 할 점이 있다.
SPI, ARRP 모두 식립시 강한 고정이 골에 과부하로 작용 할 수 있으므로 임플란트를 뒤로 다시 돌려 회사에서 제공하는 토크 조절이 가능한 라쳍을 이용하여 10-40Ncm범위에 맞춰 최종 식립 토크를 조절해 주어야 수술 시 식립 토크와 관련된 과부하를 피할수 있다.
Arrow 임플란트는 작은 직경의 임플란트 이지만 임상적인 성공률에 확신을 가져도 좋다. 작은 직경의 임플란트가 예지성 있는 높은 성공률을 가진다는 점이 치과의사들을 행복하게 해준다.